前言
許多進(jìn)入臨床應(yīng)用或臨床試驗(yàn)的藥物都起源于斑馬魚����,然而至今為止,這種小動物卻鮮有人知。由于斑馬魚的疾病特征、病因和進(jìn)展以及分子機(jī)制與臨床相關(guān)且高度保守�,斑馬魚在發(fā)育生物學(xué)方面的貢獻(xiàn)已得到公認(rèn)��,并已成為人類疾病的一個(gè)強(qiáng)有力的臨床前模型�。在生理相關(guān)劑量范圍內(nèi),斑馬魚對藥物分子的反應(yīng)與人類高度一致�,復(fù)雜的基因編輯技術(shù)加上實(shí)時(shí)高分辨率成像可以觀察到藥物分子在斑馬魚疾病模型中前所未有的分子細(xì)節(jié)。至關(guān)重要的是�����,以斑馬魚為模型的疾病通常代表人類疾病的真實(shí)模型�,可捕捉疾病的病因、進(jìn)展和解決過程。以此用來進(jìn)行活體藥物篩選���、藥理藥效評價(jià)、安全性評價(jià)和藥物代謝動力學(xué)非常高效且成本低廉����。斑馬魚模型在國外已經(jīng)被多家大型制藥企業(yè)廣泛使用于早期藥物發(fā)現(xiàn)。在此我們將討論斑馬魚如何成為藥物發(fā)現(xiàn)的重要模型以及在醫(yī)學(xué)發(fā)現(xiàn)中斑馬魚的巨大商業(yè)化潛力�。
斑馬魚(Danio rerio)因其身上的條紋而得名,是小型(2-5厘米)熱帶淡水魚�����,生活在亞洲南部的河流中�。40年前,斑馬魚作為發(fā)育生物學(xué)模式動物進(jìn)入了實(shí)驗(yàn)室環(huán)境���。斑馬魚與人類基因同源性達(dá)87%(小鼠與人類基因同源性為90%)��,由于其具有易飼養(yǎng)�����、繁殖力強(qiáng)�、發(fā)育快、受精卵透明易觀察等特點(diǎn)�����,現(xiàn)已成為在全世界范圍內(nèi)被廣泛應(yīng)用的脊椎實(shí)驗(yàn)動物�����。
復(fù)雜的基因編輯加上實(shí)時(shí)高分辨率成像���,可以前所未有的分子細(xì)節(jié)和分辨率對疾病發(fā)展過程進(jìn)行捕捉以及疾病的建模�。至關(guān)重要的是�����,對斑馬魚進(jìn)行精確的基因編輯可以生成人類疾病等位基因的模型���,在斑馬魚身上建模的疾病通常代表了人類疾病的真實(shí)模型�,捕捉了疾病的病因?qū)W�����、進(jìn)展和解決過程����,廣泛應(yīng)用于各種癌癥��、遺傳病�、肝臟疾病�、心腦血管疾病��、血液疾病����、心臟病、行為障礙�����、中樞神經(jīng)系統(tǒng)疾病等等����。
人類和斑馬魚之間的疾病蛋白和發(fā)病過程是保守的,這意味著在人體內(nèi)發(fā)揮活性的藥物分子通常在斑馬魚體內(nèi)有相同的靶標(biāo)���,特別是與靶蛋白活性區(qū)域相互作用的藥物���,這在針對癌癥以及遺傳病途徑設(shè)計(jì)的藥物中尤其顯著�����,比如MEK抑制劑等靶向療法���;以及日常常備藥物如對乙酰氨基酚、5 -羥色胺調(diào)節(jié)劑�;當(dāng)然,也存在在斑馬魚體內(nèi)有效但在人體內(nèi)無效或者在人體內(nèi)有效但在斑馬魚中無效的現(xiàn)象���,這需要在藥物發(fā)現(xiàn)階段運(yùn)用多個(gè)模型互相驗(yàn)證����。但總的來說�,在斑馬魚體內(nèi)呈現(xiàn)生物活性的藥物分子在小鼠和人體系統(tǒng)中也具有同樣的藥物特性。最近�����,小分子藥物篩選除了在胚胎時(shí)期進(jìn)行��,也已經(jīng)在成年魚身上大規(guī)模進(jìn)行�,體內(nèi)篩選的能力加上表型與人類疾病的相關(guān)性,使斑馬魚成為全動物化學(xué)遺傳學(xué)和藥物發(fā)現(xiàn)的主要模式動物���。
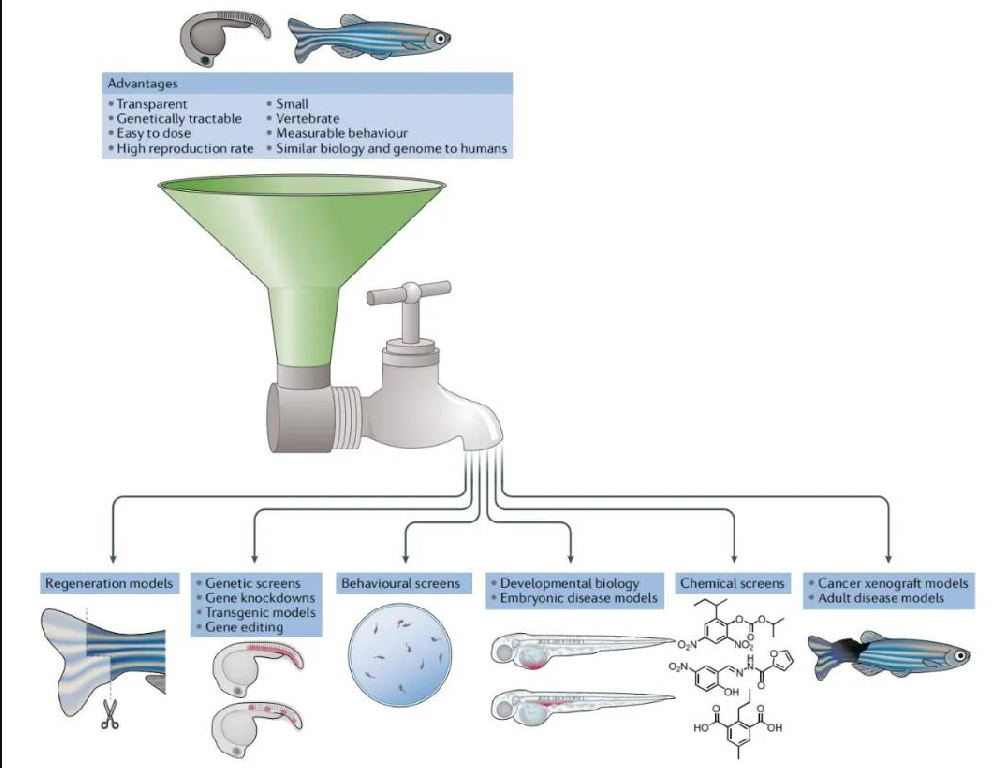
斑馬魚作為模型系統(tǒng)的優(yōu)點(diǎn)可以應(yīng)用于胚胎和成年階段的人類疾病和藥物治療模型�。數(shù)百個(gè)透明的斑馬魚胚胎很容易進(jìn)行基因編輯、轉(zhuǎn)基因和藥物篩選���。在這些胚胎階段����,器官和組織的生物學(xué)功能可以遵循活體動物的單細(xì)胞分辨率�����,以研究各種復(fù)雜的過程���,包括發(fā)育生物學(xué)、發(fā)育疾病模型���、干細(xì)胞和再生�、神經(jīng)回路和行為�����。
這篇發(fā)表于Nat Rev Drug Discov的綜述由愛丁堡大學(xué)���、哈佛大學(xué)���、麻省綜合研究所�、麻省總醫(yī)院����、哈佛干細(xì)胞研究所聯(lián)袂推出,討論了利用斑馬魚建立疾病模型的最新進(jìn)展�,強(qiáng)調(diào)了這種模式動物在藥物發(fā)現(xiàn)、探索藥物機(jī)制方面的潛力和作為臨床前藥物的全動物模型的實(shí)用性�。
一、斑馬魚表型藥物篩選
藥物發(fā)現(xiàn)的一個(gè)基本挑戰(zhàn)是顯示其有效性和理解在活體全動物系統(tǒng)中的作用機(jī)制����。盡管許多化合物和藥物先導(dǎo)藥物在體外篩選或細(xì)胞系統(tǒng)中都有活性, 但到了人體則失敗率極高����,可見體外篩選有非常大的偏差。藥物發(fā)現(xiàn)成功率51%�����,臨床前研究成功率31.8%�����,進(jìn)入臨床則成功率陡降至19.3%,現(xiàn)有的體外篩選模型在人體上的療效或安全性不佳導(dǎo)致藥物研發(fā)失?�。〝?shù)據(jù)來源:觀研天下)����,致使藥物研發(fā)長周期、高風(fēng)險(xiǎn)����、高投入。
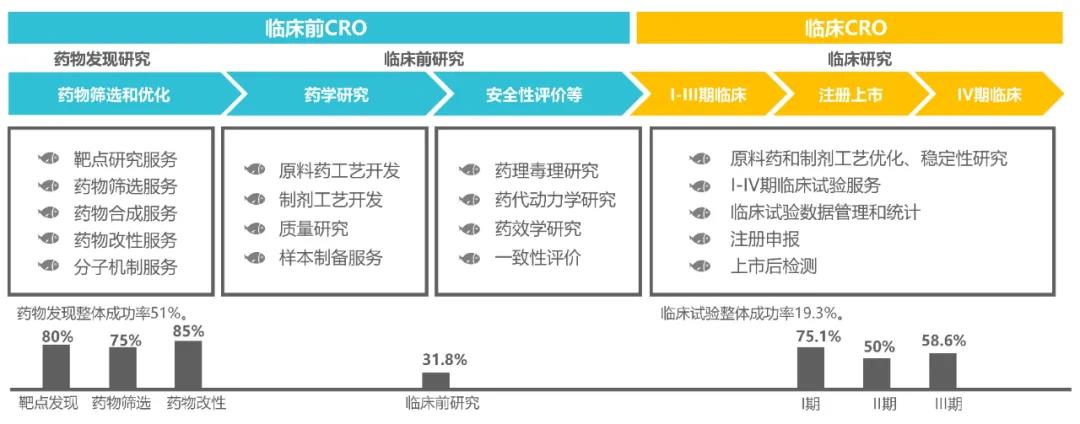
斑馬魚模型是藥物發(fā)現(xiàn)“體內(nèi)篩選”模式動物���,在快速提供精準(zhǔn)藥效、藥理結(jié)果的同時(shí)���,在初篩階段即可對先導(dǎo)化合物的吸收�����、分布�����、代謝���、毒性進(jìn)行早期評價(jià)�����,實(shí)現(xiàn)“早期失敗��,早期淘汰”����,避免將可能失敗的候選藥物帶入后期研發(fā)��,極大地節(jié)省了時(shí)間和成本�����。
通過斑馬魚模型可了解藥物在器官�、組織和身體遠(yuǎn)端部位疾病的背景下如何發(fā)揮作用,在疾病發(fā)生和治療階段監(jiān)測藥理反應(yīng)���,并評估藥物引起的不良反應(yīng)��。
01 斑馬魚模式動物的表型分析
表型藥物篩選是藥物發(fā)現(xiàn)的歷史基礎(chǔ)��,隨著靶向藥物發(fā)現(xiàn)的成功�����,表型藥物篩選再次出現(xiàn)���。表型篩選過程的內(nèi)在特征包括:即使藥物或先導(dǎo)化合物通過靶向多個(gè)靶點(diǎn)產(chǎn)生了預(yù)期的表型結(jié)果�����,它們也可以被斑馬魚模式動物識別����。例如����,激酶抑制劑可以通過靶向多種激酶產(chǎn)生治療效果。
斑馬魚胚胎的小尺寸意味著可以篩選成千上萬的活體胚胎的表型效應(yīng)�����,盡管表型斑馬魚篩選方法不如細(xì)胞���、酵母或酶體外活性測試的通量高����,但斑馬魚胚胎的篩選規(guī)模遠(yuǎn)遠(yuǎn)超過所有其他脊椎動物系統(tǒng)中可用的規(guī)模�。小分子化合物能被斑馬魚胚胎從水中直接吸收、通過鰓被成魚吸收��、或者灌胃給藥吸收����。
大多數(shù)體外高通量藥物篩選的目標(biāo)是確定具有單一靶點(diǎn)的高選擇性藥物,然而��,許多藥物作用于多個(gè)靶點(diǎn)�,影響多個(gè)生物學(xué)途徑。藥物或小分子與多個(gè)靶點(diǎn)結(jié)合的能力——多向藥理學(xué)�,正被納入藥物設(shè)計(jì),以有目的地開發(fā)針對“協(xié)同靶點(diǎn)組合”的藥物�。例如用于治療II型多發(fā)性內(nèi)分泌瘤的AD57,就是一個(gè)具備多向藥理學(xué)特性的抗癌候選藥物���。II型多發(fā)性內(nèi)分泌瘤是由激活編碼受體酪氨酸激酶超家族��、原癌基因Ret的基因突變引起的�,AD57對腫瘤患者生存期的影響是通過抑制Ret、Raf����、Src和S6K幾種激酶介導(dǎo)的,而毒性是通過抑制Tor引起的����,通過合理的化學(xué)設(shè)計(jì),設(shè)計(jì)出無Tor抑制活性但提高了Ret����、Raf、Src�、S6K抑制活性的候選藥物,提高了對II型多發(fā)性內(nèi)分泌瘤的療效并降低了毒性����。
在斑馬魚中,多維表型是指化學(xué)物質(zhì)誘導(dǎo)的表型可以幫助科學(xué)家識別并追蹤該化合物的多個(gè)靶點(diǎn)���。例如��,基于斑馬魚與其他銅螯合劑和MEK抑制劑的共同表型和酵母化學(xué)-遺傳特征��,確定了MEK抑制劑U0126既是銅螯合劑又是MEK抑制劑。
斑馬魚篩選也開始納入多靶點(diǎn)藥物的機(jī)制研究,這在基于行為的大規(guī)模表型篩選中特別有效��。例如���,科學(xué)家分析了結(jié)構(gòu)多樣化的化合物和相關(guān)的斑馬魚行為特征����,以識別具有復(fù)雜的多向藥理學(xué)機(jī)制的化合物����,如氟哌啶醇,證明其通過多個(gè)靶點(diǎn)機(jī)制提供抗精神病作用����。
對于某些藥物,斑馬魚在人體上的重現(xiàn)效果比在小鼠模型上更好�。沙利度胺的情況就是很好的例子:這種藥物被用來治療孕婦的惡心癥狀,但導(dǎo)致數(shù)千名未出生的嬰兒出現(xiàn)出生缺陷�����。在小鼠實(shí)驗(yàn)中�����,沙利度胺沒有引起任何缺陷,然而在斑馬魚實(shí)驗(yàn)中��,沙利度胺會導(dǎo)致與人類相同的肢體形態(tài)缺陷����。在這兩個(gè)物種中,沙利度胺結(jié)合并激活E3泛素連接酶CUL4-RBX1-DDB1-CRBN(被稱為CRL4)��,通過斑馬魚模式動物對沙利度胺作用靶點(diǎn)的了解解釋了該藥對發(fā)育中的胎兒的嚴(yán)重影響���,并使沙利度胺在新適應(yīng)癥(骨髓瘤)上起死回生�。
02 全動物綜合生理學(xué)
斑馬魚與人類有著幾乎相同的組織發(fā)育和內(nèi)穩(wěn)態(tài)����,包括血液、肌肉���、心臟���、肝臟、胰腺�����、脾臟、腸道���、腎臟、骨骼����、脂肪以及神經(jīng)元和神經(jīng)嵴譜系等的發(fā)育。
藥物可以在斑馬魚中進(jìn)行活體篩選�����,篩選藥效的同時(shí)提供了關(guān)于化合物的吸收����、分布、代謝����、排泄、毒性(ADME-tox)的性質(zhì)��。在目標(biāo)組織中建立化合物活性譜�����,同時(shí)測試對其他組織的影響可以整合到迭代化學(xué)中以進(jìn)行化合物開發(fā)和特異性研究。該方法提供了有關(guān)藥物或藥物組合藥理藥效和常見副作用的重要信息�����,包括因嚴(yán)重毒性而被限制應(yīng)用的救命藥物��。例如�,多柔比星是一種拓?fù)洚悩?gòu)酶II抑制劑,在殺死癌細(xì)胞方面非常有效����,但伴隨心臟毒性和心力衰竭的巨大風(fēng)險(xiǎn)。這些相同的心臟毒性在斑馬魚中均能觀察到�,通過藥物篩選發(fā)現(xiàn)了預(yù)防多柔比星誘導(dǎo)的心肌病的治療方案,發(fā)現(xiàn)了天然產(chǎn)物甲氧呋豆素��,它可以在不改變多柔比星對癌細(xì)胞的細(xì)胞毒性的情況下預(yù)防心肌病�����。最近��,這一綜合生理學(xué)的潛力得到了進(jìn)一步開發(fā)���,利用斑馬魚識別能夠防止順鉑劑量限制毒性的化合物����。順鉑是一種常見的廣譜化療藥物,可導(dǎo)致腎損傷和耳聾����。通過對腎臟和側(cè)線細(xì)胞進(jìn)行雙管齊下的毒性反篩選試驗(yàn),發(fā)現(xiàn)多巴胺及其相關(guān)的調(diào)節(jié)因子具有耳保護(hù)作用���,在不影響順鉑誘導(dǎo)神經(jīng)母細(xì)胞瘤或口腔鱗狀細(xì)胞癌細(xì)胞死亡的情況下,具有腎保護(hù)作用����。可見�����,斑馬魚模式動物在聯(lián)合用藥方案中起到了至關(guān)重要的作用�����。
03 藥物篩選
最早的斑馬魚藥物篩選僅僅是基于斑馬魚胚胎的發(fā)育表型��,這一強(qiáng)有力的方法鑒定了世界上第一個(gè)骨形態(tài)發(fā)生蛋白(BMP)抑制劑��,目前正在進(jìn)行臨床試驗(yàn)。斑馬魚系統(tǒng)跨越了整個(gè)藥物研發(fā)過程�����,從發(fā)現(xiàn)階段的高通量篩選到用于治療的臨床前藥理����、藥效、安評模型��。斑馬魚模型將成為藥物發(fā)現(xiàn)和藥物應(yīng)用的臨床前平臺��。人類基因數(shù)據(jù)與斑馬魚模型相結(jié)合�����,已經(jīng)篩選出治療淋巴異常和動靜脈畸形患者的MAPK抑制劑�,在Dravet綜合征中篩選到clemizole和lorcaserin,并均已經(jīng)進(jìn)入臨床II期試驗(yàn)階段��。斑馬魚藥物篩選和疾病模型已經(jīng)使斑馬魚在藥物發(fā)現(xiàn)和開發(fā)管線中站穩(wěn)腳跟�����,并使斑馬魚能夠?yàn)槲磥淼闹委熥龀龈匾呢暙I(xiàn)。目前����,斑馬魚模型可以覆蓋多種疾病類型,包括腫瘤����、遺傳病、心腦血管疾病���、血液疾病��、中樞神經(jīng)系統(tǒng)疾病、皮膚病和美容����、再生醫(yī)學(xué)與器官再造、肝臟疾病���、心臟病��、骨骼疾病����、行為障礙等。除此之外還在化妝品�、保健食品、食品安全����、環(huán)境監(jiān)測中廣泛應(yīng)用,這些應(yīng)用不列入本次綜述的討論����。
化合物可以在時(shí)間上有條件地影響斑馬魚發(fā)育路徑,而且表型是劑量依賴的�����。在不同發(fā)展階段添加化合物可觀察其對特定發(fā)育或疾病某一時(shí)間窗內(nèi)的生理活性����,觀察藥物如何隨著時(shí)間的推移,在整個(gè)斑馬魚的生命周期中改變細(xì)胞和組織生理學(xué)����,并提供了化合物對器官間生理、脫靶或毒性作用的證據(jù)�,以提高先導(dǎo)藥物篩選的命中率,并減少假陰性的數(shù)量����。
全動物斑馬魚篩選試驗(yàn)?zāi)軌蛟趩渭?xì)胞分辨率下對器官和組織的藥物活性進(jìn)行深度表型分析���。全面的篩選提供了捕獲發(fā)育生物學(xué)、細(xì)胞增殖�����、癌癥�����、感染和免疫�����、行為和毒性等動態(tài)的多種分析���。例如,通過使用抗體(如磷酸化組蛋白- h3抗體)篩選可以在發(fā)育胚胎的單細(xì)胞水平上跟蹤蛋白質(zhì)的表達(dá)或在采用整體熒光原位雜交(如crestin RNA表達(dá))跟蹤基因表達(dá)����;還可以利用斑馬魚從干細(xì)胞群體中再生組織的非凡能力進(jìn)行干細(xì)胞藥物篩選,包括毛囊細(xì)胞的再生�����、色素細(xì)胞再生、骨骼和脊髓再生等等���。
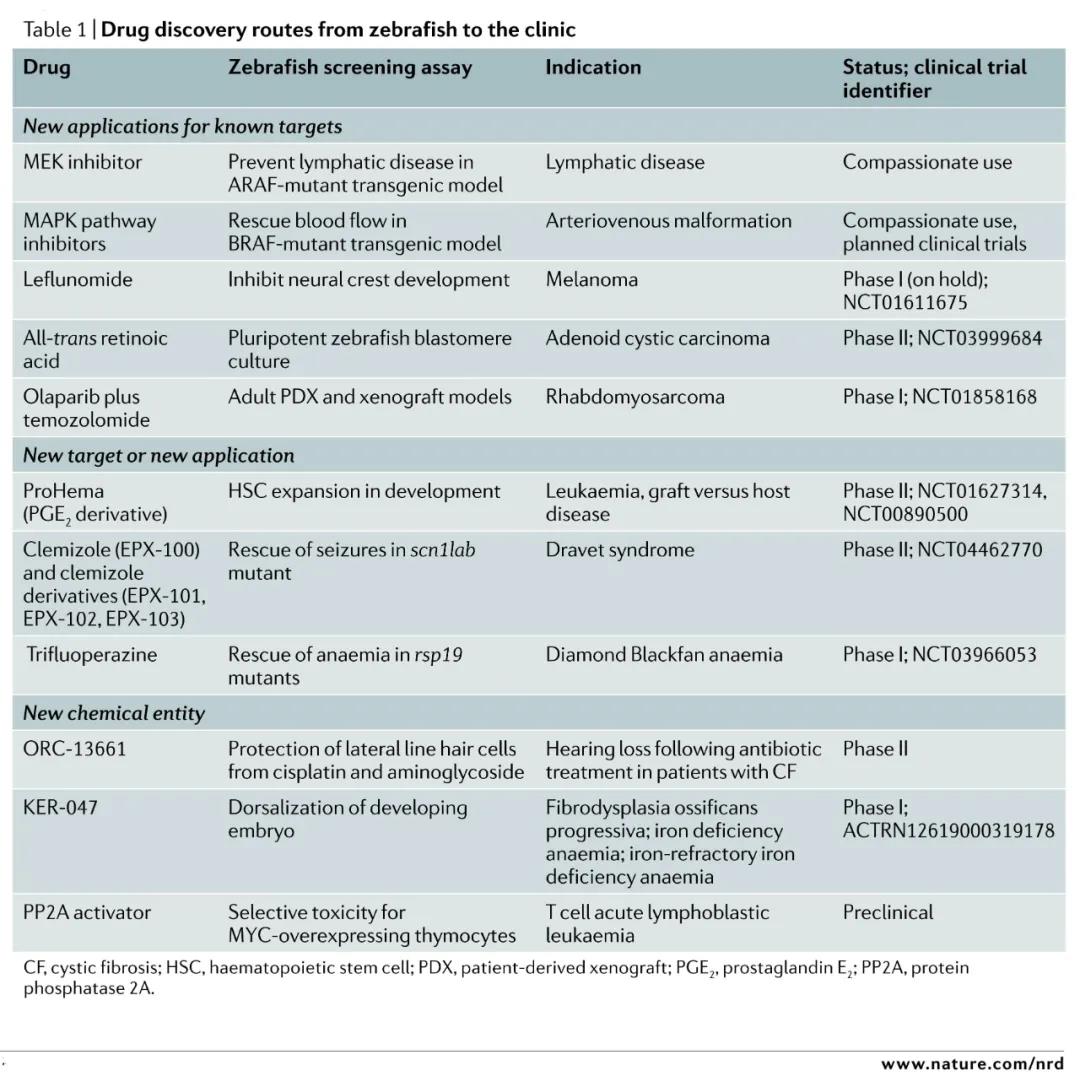
通過斑馬魚模式動物篩選的藥物已經(jīng)有多種�,但是這個(gè)方法卻不被國內(nèi)所熟知�。維渡縱橫列舉一部分通過斑馬魚模式動物篩選而發(fā)現(xiàn)的新藥案例:
熒光報(bào)告系統(tǒng)
在藥物篩選中,單細(xì)胞和組織也可以使用熒光報(bào)告系統(tǒng)在活體胚胎中篩選����。例如,使用基因熒光定量表達(dá)作為讀取器對胰腺β細(xì)胞的調(diào)節(jié)因子進(jìn)行篩選��,發(fā)現(xiàn)了組蛋白去乙?�;福℉DAC)抑制劑的全新分子����,可以降低斑馬魚的葡萄糖水平甚至在高血糖的情況下,這些抑制劑被證明在小鼠和人類β細(xì)胞模型中具有同樣的功能����。
共聚焦顯微鏡掃描
使用熒光報(bào)告分析進(jìn)行高通量篩選,通過低分辨率顯微鏡或平板閱讀器即可完成��,算然這限制了篩選試驗(yàn)的細(xì)胞分辨率,但是自動化����、高分辨率的胚胎活體藥物篩選圖像分析平臺已經(jīng)解決了這個(gè)問題。這個(gè)平臺被用來篩選調(diào)節(jié)髓鞘化少突膠質(zhì)細(xì)胞的小分子藥物�����,這些小分子藥物對軸突絕緣和支持中樞神經(jīng)系統(tǒng)至關(guān)重要���。在這個(gè)裝置中�����,斑馬魚胚胎被自動從液體中的多孔板中取出���,并通過旋轉(zhuǎn)的薄壁玻璃毛細(xì)管拉出,被旋轉(zhuǎn)圓盤共聚焦顯微鏡掃描��,這種方法不損害胚胎�,使高通量�、復(fù)雜、深度表型機(jī)制的藥物在體內(nèi)篩選更容易���。
可見表型篩選
篩選可見表型也可以用于復(fù)雜的心血管生物學(xué)和相關(guān)疾病����。斑馬魚的心臟清晰可見,在發(fā)育48小時(shí)內(nèi)血液循環(huán)活躍���。斑馬魚幼體可表現(xiàn)出心血管疾病的關(guān)鍵指標(biāo)�,包括心肌病�、心律失常和血管生成改變。這些特征使得對斑馬魚進(jìn)行脊椎動物全器官功能的藥物篩選成為可能���。心血管疾病是全球主要的死亡原因之一��,目前心血管藥物的發(fā)現(xiàn)呈下降趨勢����,斑馬魚藥物篩選有可能揭示新的�����、意想不到的心血管生物學(xué)和治療藥物線索�����。
斑馬魚的肝臟疾病與人類的疾病相似,甚至在胚胎階段也是如此����,斑馬魚胚胎的透明特性實(shí)現(xiàn)了肝臟功能的動態(tài)讀數(shù)。斑馬魚肝臟疾病模型擴(kuò)展到對乙酰氨基酚引起的毒性��,這是藥物性肝毒性最常見的原因之一�����。通過對斑馬魚胚胎的小分子篩選���,發(fā)現(xiàn)前列腺素E2(PGE2)和n -乙酰半胱氨酸(n - acetyl半胱氨酸)可以降低胚胎和成人對乙酰氨基酚肝毒性�。
斑馬魚胚胎在發(fā)育3天后就開始游動����,快速發(fā)育的數(shù)百個(gè)自由游動的斑馬魚胚胎為觀察復(fù)雜的斑馬魚行為提供了巨大機(jī)會。斑馬魚具有進(jìn)化保守的動機(jī)和決策神經(jīng)網(wǎng)絡(luò)�����,其行為分析是表型分析之一���,而這些都可以用高速相機(jī)大規(guī)模捕捉到��。斑馬魚和人類的神經(jīng)藥理學(xué)高度類似���,已經(jīng)確定了100種余種斑馬魚胚胎行為是和人類行為一致的,可以作為中樞神經(jīng)系統(tǒng)藥物篩選平臺��,包括精神障礙��、睡眠-覺醒周期�、抑郁和焦慮、癲癇和神經(jīng)退行性疾病�����、帕金森����、阿爾茲海默癥等。
可見表型結(jié)合熒光報(bào)告系統(tǒng)
表型分析可以與斑馬魚的熒光報(bào)告分析相結(jié)合�����。最近�,一項(xiàng)利用斑馬魚胚胎熒光報(bào)告基因和可見表型篩選晝夜節(jié)律調(diào)控分子的研究發(fā)現(xiàn)了非甾體抗炎藥 (NSAIDs) 和糖皮質(zhì)激素類藥物,對炎癥藥物如何改變控制日常生理和代謝健康的晝夜節(jié)律產(chǎn)生影響���。值得注意的是��,抗炎和促炎化合物的作用在細(xì)胞培養(yǎng)中是不存在的����,斑馬魚胚胎在這個(gè)復(fù)雜的生物過程中展現(xiàn)了前所未有的優(yōu)勢。
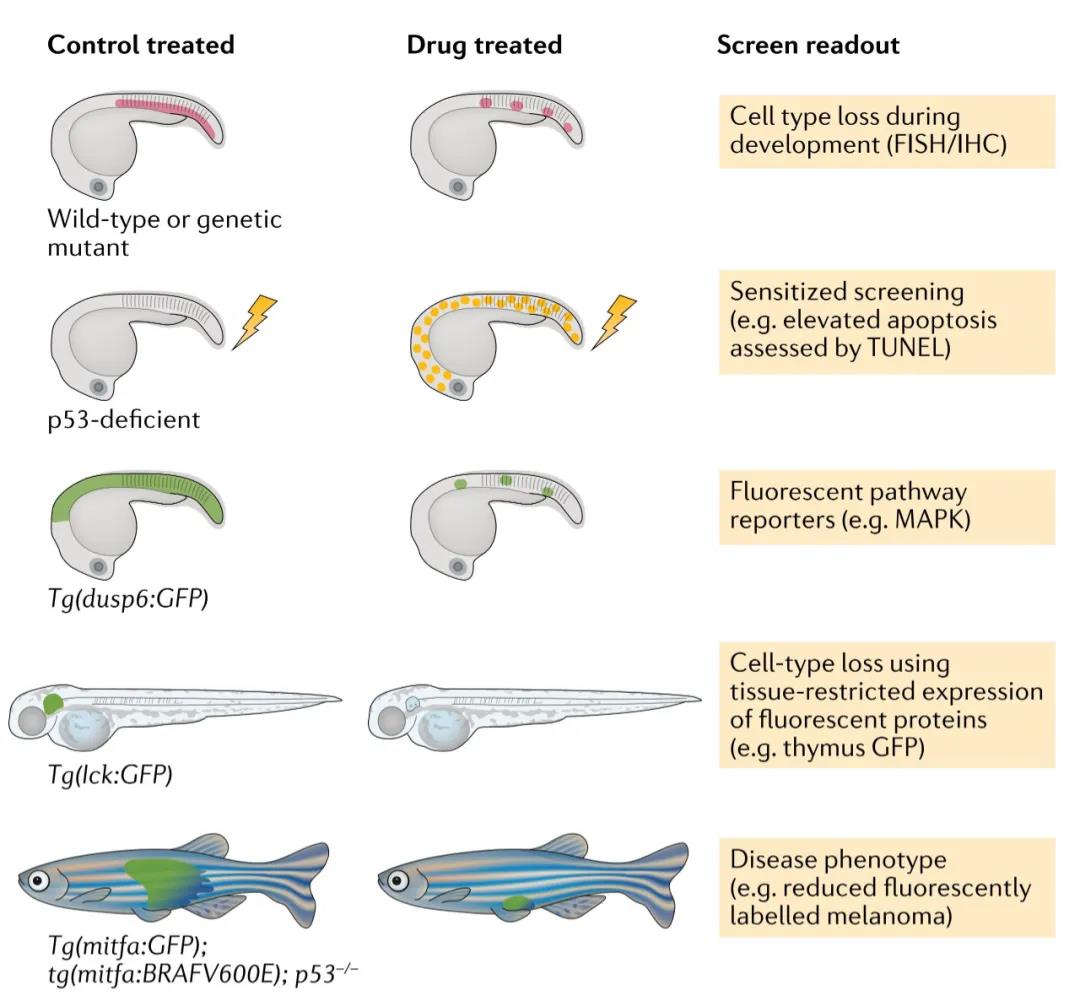
用于斑馬魚表型分析的藥物篩選方法舉例
熒光原位雜交(FISH)��、免疫組織化學(xué)(IHC)或組織特異性熒光轉(zhuǎn)基因表達(dá)可用于鑒定在胚胎����、幼蟲和成年斑馬魚中消融特定細(xì)胞類型(包括癌細(xì)胞)的藥物。致敏篩選使用遺傳突變動物或者是出現(xiàn)給藥后表型的逆轉(zhuǎn)���。在所提供的例子中����,當(dāng)通過全安裝末端脫氧核苷酸轉(zhuǎn)移酶dUTP缺口末端標(biāo)記(TUNEL)評估時(shí)�,可以鑒定出使p53缺陷胚胎對輻射誘導(dǎo)的細(xì)胞殺傷敏感的小分子。閃電表示DNA受損�����,如輻射?��?梢允褂棉D(zhuǎn)基因方法����,其中熒光蛋白在由特定分子途徑激活的基因啟動子的控制下表達(dá)����。例子中���,DUSP6是RAS途徑活性的一個(gè)眾所周知的靶標(biāo)����,可用于鑒定該途徑中的抑制藥物�����。
二����、從斑馬魚到人類疾病治療
在過去的15年里,斑馬魚的化學(xué)生物學(xué)進(jìn)展迅速��。藥物篩選的許多最初的障礙已經(jīng)得到解決。藥物發(fā)現(xiàn)科學(xué)家與臨床科學(xué)家��、藥物化學(xué)家�、制藥業(yè)將緊密互動,將化合物從實(shí)驗(yàn)室轉(zhuǎn)移到臨床應(yīng)用����,將開啟斑馬魚模式動物藥物發(fā)現(xiàn)時(shí)代的新紀(jì)元。
01 藥物發(fā)現(xiàn)高通量篩選
斑馬魚的高通量藥物篩選多選用斑馬魚胚胎模型����。科學(xué)家將斑馬魚胚胎排列到多孔板中��,每個(gè)孔包含不同的化合物或者化合物組合或中藥提取物����。斑馬魚胚胎可以在生理藥物濃度下主動吸收上述分子,通過熒光報(bào)告基因或其他表型分析來篩選起作用的化合物���,即先導(dǎo)化合物�����。確定了先導(dǎo)化合物后�����,可以通過斑馬魚模型評估藥效藥理����、毒性反應(yīng)、吸收����、分布���、代謝��、排泄�����,并通過斑馬魚胚胎構(gòu)效關(guān)系分析 (SAR) 快速優(yōu)化先導(dǎo)化合物的衍生物�����,獲得最優(yōu)的候選藥物�。候選藥物通過轉(zhuǎn)基因小鼠模型或異種移植模型進(jìn)行體內(nèi)研究���,再配合比格犬�、猴子等模式動物研究結(jié)果,候選藥物進(jìn)入人體臨床試驗(yàn)�,通過臨床I期、臨床II期�、臨床III期后成為真正的藥品上市銷售。
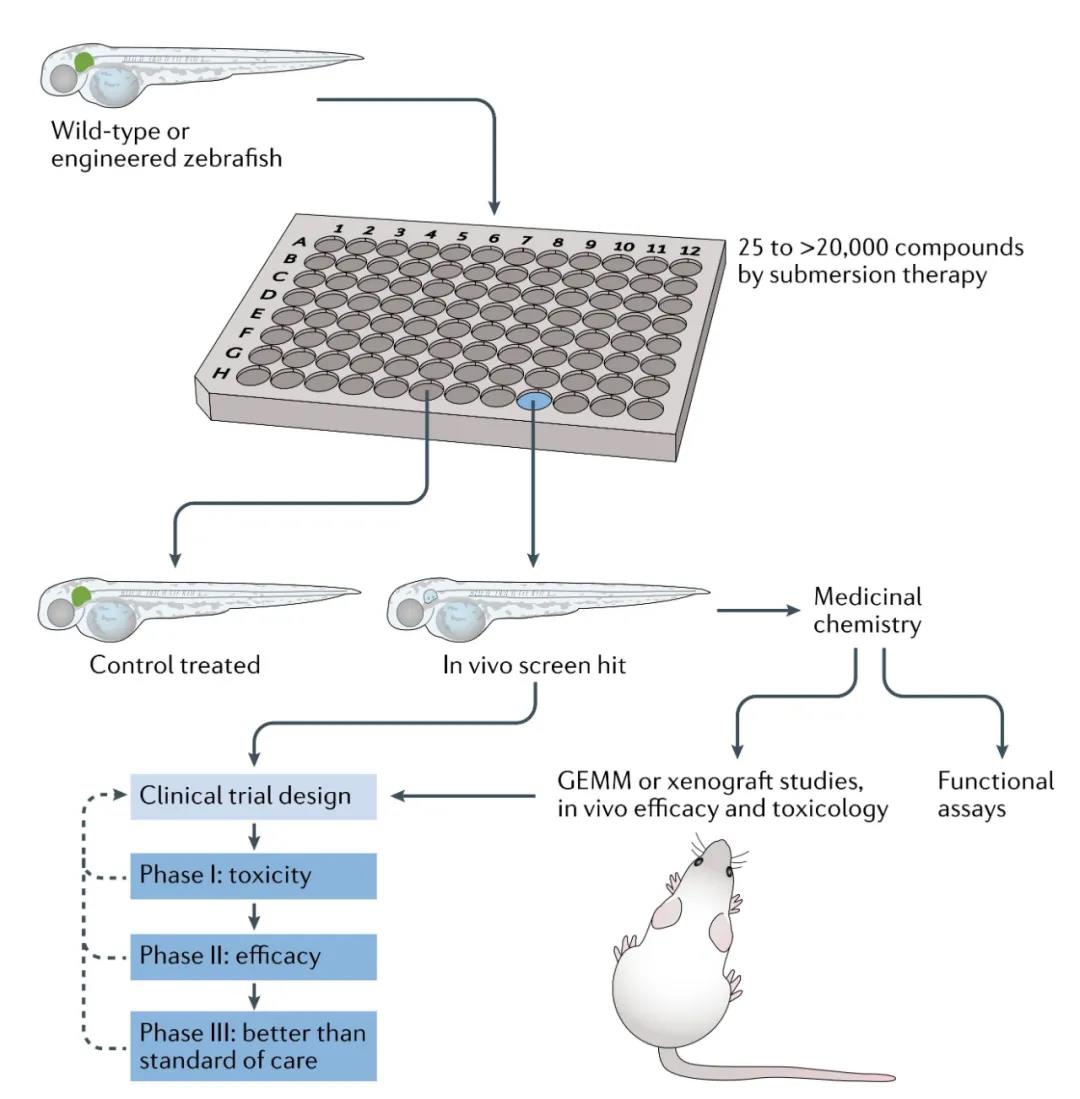
斑馬魚的藥物發(fā)現(xiàn)到臨床優(yōu)化過程
02 靶標(biāo)確證和作用機(jī)制研究
表型篩選的優(yōu)點(diǎn)之一是藥物的分子靶標(biāo)不需要已知�,也不需要假設(shè)其在疾病中的作用。對于靶標(biāo)未知的化合物�,確定其作用機(jī)制的一種技術(shù)是將藥物誘導(dǎo)的表型與已知的基因誘導(dǎo)表型進(jìn)行比較,確證靶標(biāo)和該藥物的作用機(jī)制��。斑馬魚模型被用于追蹤或發(fā)現(xiàn)藥物靶標(biāo)據(jù)有獨(dú)特的天然優(yōu)勢�。
例如,2021年12月7日�����,同濟(jì)大學(xué)宋建人團(tuán)隊(duì)在Nature Communications雜志上以題目“An injury-induced serotonergic neuron subpopulation contributes to axon regrowth and function restoration after spinal cord injury in zebrafish”發(fā)表了研究論文����,系統(tǒng)的解析了脊髓中央模式產(chǎn)生器在脊髓損傷后的修復(fù)規(guī)律,揭示了脊髓內(nèi)源性的五羥色胺參與的促進(jìn)神經(jīng)軸突再生修復(fù)的機(jī)制����,并找到了參與該修復(fù)機(jī)制的內(nèi)源性新靶點(diǎn)��,為脊髓損傷的基礎(chǔ)研究和治療提供了新的思路��。
三���、轉(zhuǎn)基因斑馬魚帶來的奇跡
轉(zhuǎn)基因斑馬魚的臨床前模型最近已成為藥物治療的熱點(diǎn),并創(chuàng)造出了奇跡��。
丹尼爾(Daniel)一出生就帶著一種罕見遺傳病——中樞傳導(dǎo)淋巴異常(central conducting lymphatic anomaly, CCLA)����。他的腿和肚子腫得像吸了水的海綿,肺部全是液體���,難以呼吸,全靠一個(gè)氧氣瓶活著����。2019年,就在費(fèi)城兒童醫(yī)院醫(yī)生Hakon Hakonarson認(rèn)為丹尼爾只有“等死”的時(shí)候�,他們發(fā)現(xiàn)了疾病的根源。他們對丹尼爾的基因進(jìn)行了測序����,包括產(chǎn)生蛋白質(zhì)的基因組——外顯子組�,以及與淋巴異常相關(guān)的十幾個(gè)基因�,結(jié)果發(fā)現(xiàn)只有X染色體上的一個(gè)名為ARAF的基因顯示不正常。然而����,ARAF突變之前從未被發(fā)現(xiàn)與淋巴疾病有關(guān)。為了證明這一點(diǎn)��,Hakonarson想到了已經(jīng)成為無數(shù)遺傳學(xué)����、發(fā)育和疾病研究的首選實(shí)驗(yàn)動物——斑馬魚。
Hakonarson將這種基因突變通過基因工程改造進(jìn)斑馬魚體內(nèi)�����,等斑馬魚形成和丹尼爾相同的病癥時(shí)���,在斑馬魚身上測試多種藥物�,如果能發(fā)現(xiàn)其中一種藥物可以阻止淋巴管的生長���,并且該藥物能獲得聯(lián)邦衛(wèi)生部門的許可��,那么就可以在兒童患者身上進(jìn)行嘗試����。
按照計(jì)劃,斑馬魚5天內(nèi)就長成了淋巴系統(tǒng)�,并給了一組ARAF突變的斑馬魚10種不同藥物?�!爸灰獙⑺幬锓湃胨?����,這些斑馬魚就能吸收藥物��?��!盨eiler說����,“不需要像用小鼠模型要一只只注射那么麻煩����?����!苯K于他們發(fā)現(xiàn)了——trametinib,一種商品名為Mekinist的黑色素瘤藥物���,研究人員將該藥物放入水中�����,斑馬魚在吸收藥物后淋巴管停止擴(kuò)散����,并且沒有對其他組織和器官造成傷害�����。
經(jīng)FDA批準(zhǔn)�,費(fèi)城兒童醫(yī)院團(tuán)隊(duì)給丹尼爾開了 trametinib。奇跡出現(xiàn)了�����。用藥2個(gè)月��,丹尼爾的呼吸得到改善�����。服藥三個(gè)月時(shí),他肺部的液體已經(jīng)消退�,不再需要另外補(bǔ)充氧氣,雙腿的腫脹也消失了���,核磁共振顯示他的淋巴管已重塑成接近正常的狀態(tài)�。據(jù)STAT報(bào)道���,這是一種藥物首次重塑整個(gè)器官系統(tǒng)����。
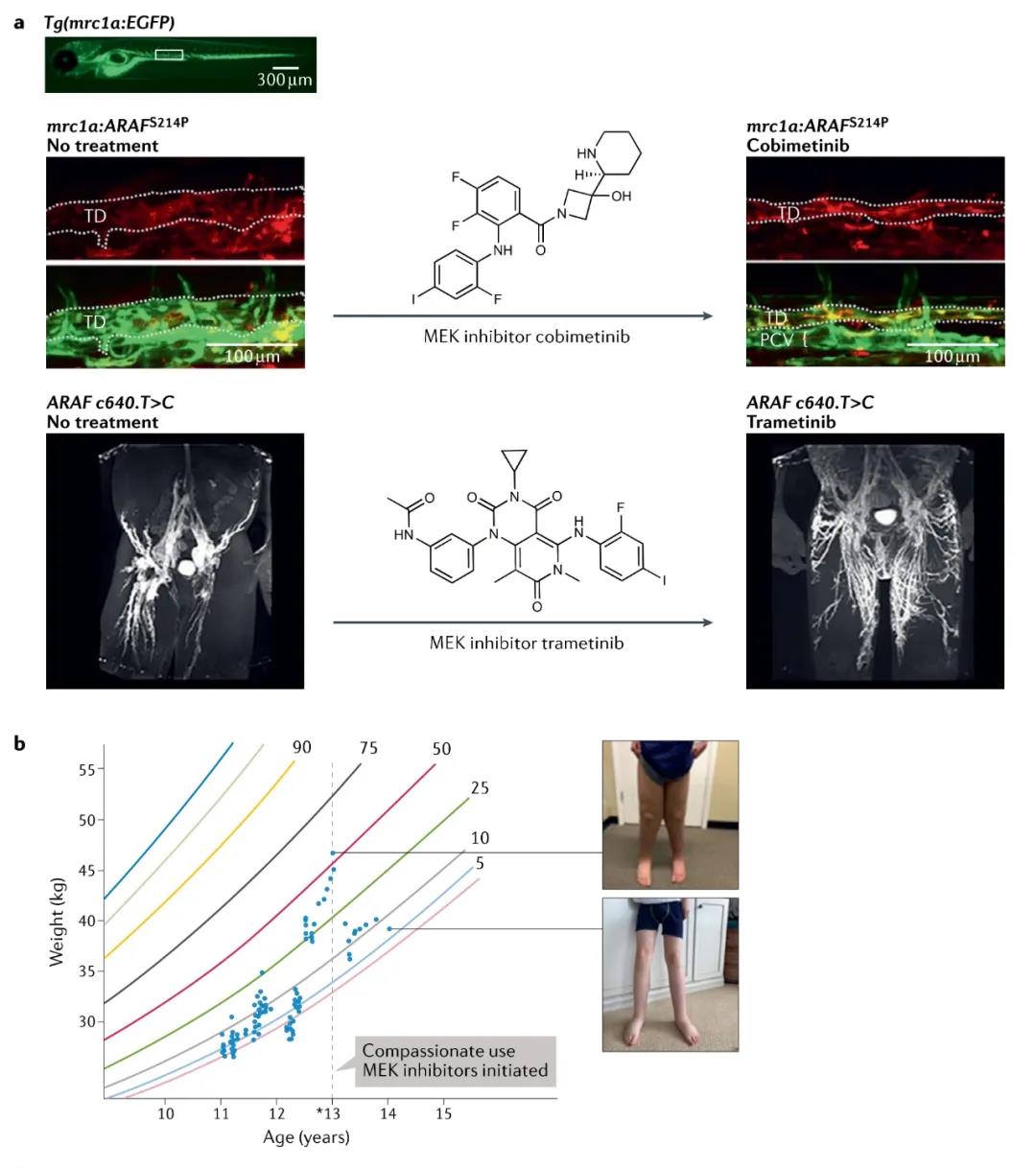
“一項(xiàng)研究可能失敗上千次���,才成功一次�����?!盨eiler說�,“但是在斑馬魚身上測試所顯示的結(jié)果能夠直接用回臨床診療中�����,這簡直太給力了?����!爆F(xiàn)在14歲的丹尼爾可以打籃球���,騎自行車�����,還幫助教練練足球����。
這項(xiàng)研究發(fā)表在2019年的《Nature Medicine》雜志上�����。

除此之外�,轉(zhuǎn)基因斑馬魚模型用于T細(xì)胞急性淋巴細(xì)胞白血病、肝細(xì)胞癌�、癌癥RAS通路等的創(chuàng)新藥物已經(jīng)紛紛進(jìn)入臨床試驗(yàn)研究。
四��、斑馬魚移植模型新突破
01 同種/異種腫瘤移植模型
使用幼體和成年魚的同種/異種移植試驗(yàn)為評估藥物在活體動物體內(nèi)對人類癌癥的治療提供了新機(jī)會。
斑馬魚移植模型分為同種異體移植模型����、幼魚的異種移植模型、免疫缺陷魚的異種移植模型���。斑馬魚異種移植模型可以進(jìn)行癌癥藥物療效的臨床前測試:可直接移植人類腫瘤移植物至斑馬魚���,形成異種移植模型進(jìn)行藥物測試。通過對魚體內(nèi)熒光腫瘤的成像�����,以及對單細(xì)胞終點(diǎn)(如細(xì)胞周期或藥物靶標(biāo)通路)的高分辨率成像�����,可以監(jiān)測藥物效應(yīng)���,可以進(jìn)一步測試其毒性�����。
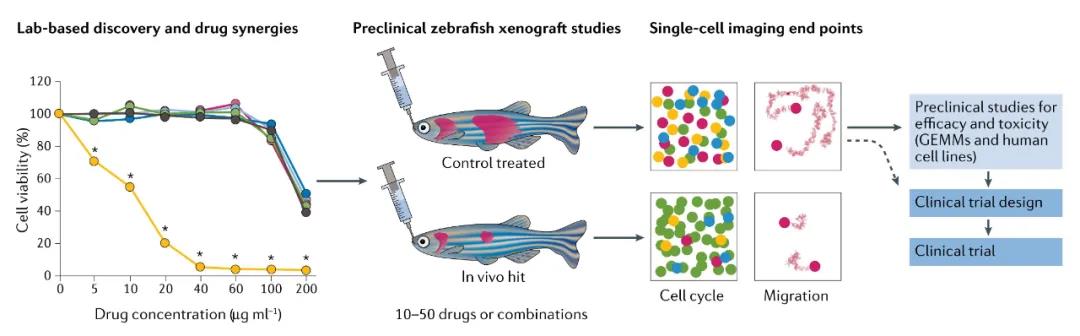
隨著基因組工程技術(shù)的發(fā)展���,已經(jīng)培育出缺乏T細(xì)胞、B細(xì)胞和自然殺傷細(xì)胞(NK)的免疫缺陷成年斑馬魚����,為“免疫缺陷魚異種移植模型”提供了基礎(chǔ)工具。這些模型的優(yōu)點(diǎn)包括能夠在37°C的環(huán)境下飼養(yǎng)魚類��、以臨床可實(shí)現(xiàn)的方式使用口服灌胃而不是浸泡療法給藥�����、以及植入足夠的細(xì)胞使其形成具有與人類患者類似的組織學(xué)和長期生長動力學(xué)的腫瘤���。
2019年�����,David M.Langenau和Yan Chuan在世界上首次培育出缺乏T細(xì)胞�����、B細(xì)胞���、NK細(xì)胞但仍能存活到成年的復(fù)合突變斑馬魚���,可以穩(wěn)定地移植多種人類癌癥,包括黑色素瘤����、三陰性乳腺癌、橫紋肌肉瘤等�����。給橫紋肌肉瘤斑馬魚移植模型灌胃給藥����,發(fā)現(xiàn)PARP抑制劑奧拉帕尼聯(lián)合替莫唑胺是一種新的人類橫紋肌肉瘤治療方法。重要的是��,這項(xiàng)工作使用了口服灌胃和給藥程序�,模擬了臨床可以達(dá)到的給藥頻率和血液水平?��;诎唏R魚藥物發(fā)現(xiàn)以及后期在PDX小鼠模型中的驗(yàn)證�����,該藥物組合現(xiàn)在已經(jīng)進(jìn)入臨床試驗(yàn)(NCT01858168)��。
02 干細(xì)胞移植
移植是測定造血干細(xì)胞(HSCs)體內(nèi)功能最常用的方法��。盡管已經(jīng)在斑馬魚中開發(fā)了各種HSC移植策略���,但由于與免疫匹配和預(yù)處理毒性相關(guān)的挑戰(zhàn),它們并未得到充分利用���。為了規(guī)避這些限制���,Teresa V.Bowman使用HSC缺陷宿主開發(fā)了一個(gè)簡單而強(qiáng)大的移植模型。該測定的簡化方法和穩(wěn)健性將有助于擴(kuò)大其未來在斑馬魚中進(jìn)行高通量移植實(shí)驗(yàn)的可行性��,并將促進(jìn)造血干細(xì)胞生物學(xué)的進(jìn)一步新發(fā)現(xiàn)��。
五�、盤點(diǎn)斑馬魚模式動物CRO

研究顯示,國外大藥廠包括諾華�、禮來、輝瑞�����、羅氏�、賽諾菲���、葛蘭素史克等均已采用斑馬魚模式動物進(jìn)行藥物發(fā)現(xiàn)研究。而當(dāng)前����,專注斑馬魚模式動物的CRO公司還不多,主要有Phylonix Pharmaceuticals���、Evotec����、Biobide����、Zeclinics、環(huán)特生物����、英創(chuàng)新藥、斑馬藥業(yè)�、羿晟生物、再本生物�����,有少量涉及該業(yè)務(wù)的CRO國內(nèi)還有南模生物。
公益性質(zhì)的包括Zebrafish Disease Models Society���。
斑馬魚模式動物CRO目前服務(wù)內(nèi)容涵蓋小分子藥����、中藥����、抗體藥���、核酸藥����、基因治療�����、化妝品���、保健品����、食品安全等的全方位服務(wù)。從環(huán)特生物官網(wǎng)來看�����,目前服務(wù)客戶呈現(xiàn)多元化�����。

六�、展望
藥物發(fā)現(xiàn)仍然是一個(gè)昂貴和費(fèi)力的過程,實(shí)驗(yàn)室研發(fā)和臨床試驗(yàn)之間巨大的科學(xué)差距加大了藥物開發(fā)的難度��。鑒于斑馬魚和人類對藥物的共同反應(yīng)���,斑馬魚與小鼠���、猴子等哺乳動物的臨床前預(yù)測模型一樣強(qiáng)大。斑馬魚和人類共同的藥理學(xué)使斑馬魚成為藥物再利用的重要伙伴����,也是發(fā)現(xiàn)新分子實(shí)體的新興工具,從而打開了新藥開發(fā)的嶄新的鑰匙�。
引用資料
[1] E. E. Patton, L. I. Zon, D. M. Langenau. Zebrafish disease models in drug discovery: from preclinical modelling to clinical trials. Nat Rev Drug Discov, 2021, 611-628.
[2] Li, D., March, M.E., Gutierrez-Uzquiza, A. et al. ARAF recurrent mutation causes central conducting lymphatic anomaly treatable with a MEK inhibitor. Nat Med. 2019, 25, 1116–1122.
[3] Yan, C. et al. Visualizing engrafted human cancer and therapy responses in immunodeficient zebrafish. Cell. 2019, 177, 1903–1914.
[4] Ellen Fraint, María Feliz Norberto, Teresa V. Bowman, A novel conditioning-free hematopoietic stem cell transplantation model in zebrafish. Blood Advances, 2020, 4, 6189-6198.
[5] ZDMC:https://www.zdmsociety.org




 17312606166
17312606166